|
BAB 1
PENDAHULUAN
1.1
Latar belakang M asalah
Dunia
industri
di
Indonesia
saat
ini
sarat
dengan
persaingan
yang
menuju
ke
arah
persaingan
global
yang
dikarenakan
oleh
perkembangan pasar
dunia
yang
semakin
global,
terutama
dalam
menghadapi
perdagangan
bebas
ASEAN
yang
dikenal
dengan sebutan
AFTA (ASEAN Free Trade Area)
pada tahun
2008
mendatang,
yang
memacu
munculnya
pemain-
pemain
baru dalam
dunia
industri,
menuntut setiap pelaku bisnis atau perusahaan-
perusahaan
untuk
terus melakukan
perbaikan
yang berkesinambungan
agar
terus
bertahan
dan
menjadi
yang terbaik.
Tantangan
lain
yang dihadapi
oleh
dunia
industri
adalah
tuntutan pelanggan
(customer),
dimana
setiap
perusahaan
akan
melakukan
apa
saja
untuk
mencapai
kepuasan
pelanggan
(customer
sat isfaction).
Salah
satu
syarat
utama
untuk
mencapai kepuasan pelanggan adalah kualitas dari produk yang dihasilkan.
Kualitas
disadari sebagai suatu
alat yang
mempengaruhi
kepuasan pelanggan
terhadap
suatu produk
dan
kemudian
akan
berpengaruh
pada kesetiaan pelanggan
terhadap
produk
tersebut,
serta
berdampak
pula
terhadap
kemajuan
dan
kelangsungan usaha bisnis
yang
bersangkutan. Kualitas
tidak
ditentukan oleh
|
|
2
pembuat, sebaliknya
kualitas adalah karakteristik suatu produk
dan
jasa yang
menunjang pada kemampuannya
untuk
memuaskan
kebutuhan
tertentu.
Peningkatan
kualitas
produk
mempunyai
tujuan
meminim asi
jumlah
produk
yang
cacat
atau
defect.
Dengan
berkurangnya
jum lah
produk
cacat,
m
aka
penanganan
terhadap
produk
cacat pun
dapat diminimasi
serta
dapat
meningkatkan
produktifitas
dan
pada akhirnya m eningkatkan
profit bagi
perusahaan.
Tak
dapat dipungkiri
lagi
bahwa
pencapaian
karakteristik
kualitas
produk
sangatlah
sulit
dilakukan
secara
konstan.
Karena
itulah,
peningkatan
kualitas
produk
secara
terus-
menerus
(continous
improvement)
perlu
dilakukan
oleh
para pelaku
bisnis
yang berdinamika dalam
dunia
industri.
Salah
satu metode
untuk
peningkatan
kualitas
adalah
TPM (Total
Produktive
Maintenance),
dim ana
PT
Dankos
Farm a
mempunyai
policy
TPM
yang
berbunyi
“PT
Dankos
Farma
bertekad
untuk
berproduksi
tanpa
gangguan
dengan
melibatkan
seluruh karyawan
dalam
kegiatan
pemeliharaan
fasilitas
produksi
guna mencapai
tingkat
produktivitas
tertinggi, bermutu
prima dan ekonomis.”
Demikian
pula halnya
dengan
PT
Dankos Farm a sebagai
salah
satu
BO
(Business
Operation)
dari
PT
Kalbe
Fama
Tbk
yang
bergerak
di
bidang
farmasi.
Produk-
produk
yang
dihasilkan
oleh
Dankos
term asuk
dalam
kategori
produk
obat
di
mana
kualitas
sangat
penting
bagi
konsumen
atau
pengguna
akhir
selain
bagi perusahaan.
Visi
perusahaan
Dankos
adalah
senantiasa
menjadi
perusahaan
farmasi
yang
berkomitmen
kuat
melalui
penerapan
ilmu
dan
teknologi
untuk
peningkatan
|
|
3
kesejahteraan
masyarakat.
Sehingga
untuk
mendukung visinya,
perusahaan
mempunyai misi
untuk
senantiasa berkomitmen
melakukan
perbaikan
yang
berkesinambungan
untuk
menghasilkan
produk kesehatan
yang berkualiats
melalui perkembangan
produk
yang
inovatif,
mudah
diperoleh
dan
terjangkau
sehingga
secara
tidak
langsung
ikut berperan
serta
dalam
meningkatkan
kesejahteraan
masyarakat.
Lebih dari
pada
itu
perusahaan
membentuk
motto
untuk
mendukung
visi
dan
misinya
dimana
mottonya
adalah
“Mutu
untuk
kesehatan
dan
Hidup
yang lebih
baik”.
Dengan
demikian
peningkatan
kualitas
merupakan
kunci sukses dalam
agenda penting bagi PT
Dankos
Farma.
1.2
Identifikasi dan Perumusan
Masalah
Dalam
menghadapi
persaingan
di tingkat
perusahaan-perusahaan
farmasi
yang
mulai
berkembang
di
Indonesia
ini,
PT.
Dankos
Farma
selalu
berpegang
teguh
dengan
Best
Practice-nya
yaitu
(Total
Productive Maintenance
(TPM),
Customer
Care,
Int ernal
Customer
Satisfaction,
Excellent
Manufacturing, 5R,
dan
Continual Improvement).
Continous
Improvement
atau
yang biasa
disebut
dengan
perbaikan
yang
berkesinambungan
bertujuan
untuk
peningkatan
produktivitas
dan dijalankan
dalam
berbagai
faktor baik
produksi,
sistem
inform asi, perkantoran
maupun
hal-
hal teknis
lainnya.
Berbagai
perbaikan
telah
dilakukan
untuk
menaikkan
nilai
produksi
dengan
cara
mempercepat
proses
produksi,
m
emperbaiki
sistem
informasi,
mengurangi
jam
kerja,
mengurangi
tenaga
kerja
dan
lain-lain
dengan
tanpa
mengurangi
kualitas
produk
itu
sendiri.
Peningkatan
produktivitas
yang
|
|
4
secara bertahap
terus-menerus
dilakukan
diperlukan
untuk
mempermudah
dalam
hal
prediksi
lamanya
proses
suatu
produksi.
Hal
ini
akan
berhubungan
dalam
hal
pemenuhan
target
(Order
Fullfilment)
yang
dikeluarkan
oleh
bagian
PPIC (Production
Planning
In
Control)
untuk
setiap
produk
dalam
setiap
bulannya.
Apabila produktivitas
meningkat,
maka
akan
mempermudah
dalam
pemenuhan
target oleh bagian produksi yang
diberikan
di
awal
bulan.
Selanjutnya
target
akan
dirubah
sesuai
dengan
kemampuan
produksi.
Pada
saat
ini
proses produksi
sulit
untuk
diprediksi,
dikarenakan
waktu
proses
yang
tidak
stabil
dan
cenderung
berubah-ubah
dalam
rentang
waktu
yang
lebar.
Sehingga
terkadang
target
yang
diberikan
oleh
PPIC
sering
tidak
terpenuhi
dikarenakan
waktu
yang
diperlukan
kurang
atau
target
yang
diberikan
terlalu
mudah
dipenuhi
sehingga
proses
produksi menjadi tidak efektif
dan efisien.
Oleh
karena
itu
perlu
dilakukannya
improvement
untuk
menyelesaikan
permasalahan
ini dengan
tanpa mengurangi kualitas dari produk
itu sendiri.
Karena
produktivitas dan
kualitas
merupakan
satu
kesatuan
yang
tidak
dapat
dipisahkan.
Dengan
dilakukannya
perbaikan
tanpa
mengurangi
kualitas
diharapkan
akan
terjadinya peningkatan
target
order
fullfilment
yang
sekaligus
akan
dapat
menambah profit sendiri
bagi perusahaan
ini.
Seperti
yang
telah diuraikan diatas bahwa proses produksi sulit
sekali
diprediksi, khususnya
pada proses
injeksi kering
yang sulit dilakukan
dalam
hal
|
|
5
penentuan
target
produksi.
Dari
pengalam an
dan
hasil
pengukuran
yang
telah
didata,
rentang variasi
waktu
proses
produksi
terlalu
lebar
sehingga
hal
ini
akan
menyulitkan
bagian
PPIC untuk
penentuan
target
itu
sendiri.
Salah
satunya
yang
akan
diangkat
dalam
hal
ini
adalah
pada
langkah
proses
produksi
injeksi
kering
di bagian produksi.
Dalam
proses
injesi
kering
terdapat
banyak
faktor
yang mempengaruhi
akan
keberhasilan
proses
produksi,
seperti
diketahui
bahwa
injeksi
kering
sangat
rentan
dengan
kondisi
lingkungan
sekitar.
Untuk
mendapatkan
hasil
maksimum
dalam
hal
ini
sterilitas
dan
kejernihan
vial
diperlukan
man
and
machine
yang
memenuhi
kreteria
CPOB
(Cara
Pembuatan
Obat
yang Baik).
Terdapat
tiga
langkah
proses
produksi
di
dalam
memproses
injeksi
kering
antara
lain
proses
pencucian
vial,
proses
sterilisasi
kering vial
dan
proses
pengisian
serbuk
injeksi
kering
ke dalam
vial, tiap proses yang berlangsung
memiliki kondisi
yang
berbeda
dan
pada akhirnya vial
yang keluar
harus
dalam
kondisi
steril
itu
adalah
syarat mutlak
di dalam
produksi
injeksi kering.
Selama ini proses
produksi
yang
berlangsung
dirasa
masih
kurang
optimal
dalam
artian
masih
jauh
dari
target
yang
telah
direncanakan,
untuk
mengetahui
apa
yang
terjadi
selama proses
produksi
maka
dilakukanlah
pengamatan
selama
beberapa
hari untuk
mengetahui
faktor-
faktor
apa
saja
ynag
menghambat
proses
produksi
dengan
demikian
diharapkan
dapat
merubah
sistem
yang
ada
diganti
sistem
yang
baru
yang lebih efektif dan
efisien.
|
|
6
Pada
umunya
konsep
peningkatan
produktivitas
dimulai
dari
satu
continous
improvement
dimana
dari
improvement
ini
secara
langsung
akan
memperbaiki
kualitas
dari proses
dan
produk
itu
sendiri,
yang
pada
akhirnya
akan
menghilangkan
berbagai
akar
penyebab
masalah
yang
ada
dalam siklus
produksi
di
perusahaan
ini.
Dengan
hilangnya
berbagai
akar
penyebab
masalah
tersebut
maka akan
terjadi
peningkatan
produktivitas
perusahaan
yang juga
akan meningkatkan
profitabilitas dari perusahaan
itu
sendiri.
Untuk
itu,
disini
peneliti
akan
mencoba untuk
mengidentifikasikan
permasalahan
yang ada
pada
bagian
produksi
terutama
line
injeksi
kering
dengan
m
enganalisa
masalah-masalah
berikut
ini
:
1.
Apa
yang
m
enjadi
faktor
utama
penyebab
munculnya
permasalahan tidak
tercapainya
target produksi untuk produk injeksi kering ?
2.
Tahapan
apa
saja
yang
merupakan
bottle
neck pada proses
produksi
injeksi
kering dan mengapa?
3.
Bagaimana
langkah
perbaikan
yang dilakukan
pada
produksi
injeksi
kering
tersebut
agar
masalah bottle neck dapat diminimalkan?
4.
Apakah target
produksi yang
telah
ditetapkan dapat
tercapai setelah
dilakukan
tindakan
perbaikan
dengan baik
dan
tepat. ?
1.3
Ruang
Lingkup
Di
sini
penulis
ingin
m
elakukan
analisa
dan
penelitian secara
TPM
pada
bagian
produksi
injeksi
kering
mulai
dari
proses
pencucian
vial,
proses
|
|
7
sterilisasi
kering
vial
dan
proses
pengisian
serbuk
injeksi
kering
ke
dalam
vial,
hal ini dilakukan
untuk
mengetahui
keefektivan
tiap proses produksi.
Untuk
m
emperjelas
arah pemecahan
masalah
yang
akan
dibahas
di
dalam
skripsi nantinya,
berikut adalah
pembatasan terhadap masalah
yang di bahas:
1. Penelitian
akan
dilakukan
pada
PT
Dankos
Farma
yang bertempat
di
kawasan
industri Pulogadung.
2.
Pengukuran
penelitian
dilakukan
pada operasional
mesin
dan
hasil
produk
dari
mesin
pencucian
vial,
mesin
sterilisasi
kering
vial
dan
mesin pengisian
serbuk
injeksi kering ke dalam
vial.
3.
Analisa
dan
pengukuran
menggunakan
metode
TPM dimana
dari
perhitungan
tersebut dapat
diketahui
time
losses
dan
performance
effeciencies
dari
tiap proses produksi.
4.
Metode
yang digunakan
untuk
mengidentifikasi
dan
menganalisis
sumber
penyebab
terjadinya permasalahan
ini
adalah
metode
FMEA
(Failure Mode and Effect Anal
ysis
).
5.
Data
yang
digunakan
untuk
m
enentukan
penyebab
terjadinya
bottle
neck
didapatkan
dengan melakukan
observasi,
wawancara
dan
brainstorming dengan pihak
perusahaan.
1.4
Tujuan dan Manfaat
Berikut ini adalah
beberapa
tujuan
yang dapat diperoleh dari penelitian
yang
dilakukan
dalam
hal peningkatan
produktivitas dengan metode TPM antara
lain:
|
|
8
1.
Menurunkan
”Down
Time
Machine”
produksi
dalam
hal
ini
ketersediaan
change part yang diperlukan
khususnya line injeksi kering.
2.
Meningkatkan
“Performance Efficiency”
Mesin
,
dapat
diketahui
dari
Time
Losses yang terjadi
dan
Actual
Yield dari masing- masing mesin.
3.
Meningkatkan
“Quality
Ratio”
Produk
,
dengan
diketahuinya
besarnya
deffect
product
tiap
batchnya
maka
dapat
dicarikan
solusi
yang
paling
optim al
yang dapat
menekan tingkat defect.
4.
Merencanaan target
tingkat
produktivitas
mesin
dimasa
datang
agar
dapat
terus
dimodifikasi
kembali
berdasarkan
informasi
hasil
dari
improvem ent
yang terus berkelanjutan
Adapun beberapa manfaat
yang dapat diperoleh dari penelitian ini antara
lain
:
1.
Mengefektifkan
peralatan
dan
mesin
khususnya
peralatan
atau
part
mesin
yang
mempunyai
umur
pakai
yang
singkat sehingga
dapat
disediakan
cadangan/ spare part.
2.
Dengan
adanya
perhitungan
Time
Losses
dan Rat e off Qualit y Product
pada
tiap proses m aka dapat dikahui
mutu produk yang dihasilkan.
3.
Perawatan
otonomi
oleh operator
yang dapat
m
eningkatkan
ketrampilan
karyawan, sehingga mengenal betul akan kondisi mesinnya.
4.
Penentuan
target produksi
dapat
dilakukan
lebih
mudah,
karena
sudah
dihasilkan
suatu standart proses
yang sudah mewakili siklus
proses
produksi.
|
|
9
5.
Dapat digunakan
sebagai
bahan
masukan
dan
menjadi
bahan
penelitian
bagi
rekan-rekan
mahasiswa/i
untuk
yang
berminat
meneliti
dengan
topik
yang
sama dengan
penulis.
1.5
Gambaran
Um um Perusahaan
1.5.1
Sejarah Perusahaan
PT.
Dankos
Farma
yang awalnya
bernama
PT.
Dankos
Laboratories
Tbk.
didirikan
pada
tanggal
25
Maret
1974
di
Pulomas,
Jakarta
Timur
yaitu
sebuah
perusahaan
farmasi
dan
merupakan
induk
dari
beberapa
anak
perusahaan
yang
bergerak
dibidang
farm asi,
memulai
kegiatan
operasinya
di
bidang
obat-
obtan
pada
tahun 1978
dengan
lahan
seluas
500
m2.
Setelah
beroperasi
selam a empat
tahun
di Pulomas,
Dankos
memindahkan
kegiatan
operasionalnya
di Kawasan
Industri Pulogadung
dengan
luas
lahan 12.800 m2 dan luas bangunan
3925 m2.
Pada tahun
1986 Dankos
mendapatkan
lisesnsi
produk
dari
Fujisawa (Jepang)
dan Daiichi
(Jepang). Produk-
produk
yang
dihasilkan
oleh Dankos
saat
ini
adalah
:
a.
Obat
Bebas
(OTC)
•
Cream
:
Trimadan
•
Granule
:
X-ion
•
Liquid
:
Mixagrip
Syrup
Stawberry & Orange
•
Tablet
:
Fatigon, Mixagrip,
Mixadin,
Mixaflu
|
|
10
b. Obat
Resep
(Ethical)
•
Cream
:
Oxyzone
•
Injeksi Kering
:
Cefizox,
Broadced,
Foxim, Cefotaxime
•
Kapsul
keras
:
Cefadroxil
500m g, Librocef
500mg,
Longcef
•
Tablet
:
Topcillin,
Kalcef, Lizor, Cefspan
Sejalan
dengan
pertumbuhan
ekonomi
Indonesia,
maka
pada
tanggal
13
November
1989,
Dankos
melakukan
go
publik
dengan
mencatatkan
sahamnya
pada
Bursa
Efek
Jakarta dan
Surabaya.
Pada
tahun
1990
Dankos
mulai
melakukan
eksport
obat
bebas
(OTC)
ke
sepuluh
negara
(Asia
dan
Afrika).
Pada tahun
yang
sama
PT.
Dankos
memperoleh
100%
saham
PT
Bintang
Toejoe.
Dankos
memperoleh
sertifikat
GMP
(Good
Manufacturing
Practice)
pada
tahun
1991.
Dankos
membangun
gedung Penicillin
dan
gedung
Cephalosporin
pada
tahun
1993
untuk
perluasan
dan
peningkatan
produksi.
Pada
tahun
yang
sama
Dankos
memperoleh seluruh
asset
PT. Hexpharm
Jaya. Pada
tahun
1995
Dankos
m
emperluas
pabriknya
menggunakan
bangunan
Ex
Helios
yang
letaknya
bersebelahan
dengan
luas
lahan
5.898
m2
dan
luas
bangunan
3.868
m2.
Dankos selalu
berkomitmen
untuk
meningkatkan
mutu
dan
kualitas
produk
yang
dihasilkan,
hal
uni
dibuktikan
dengan
menjadi
Industri
Farmasi
Indonesia
yang pertama
kali
memperoleh sertifikat ISO
9001
pada tahun
1997,
perbaikan
yang
berkesinambungan,
5R (Ringkas,
Rapi,
Resik,
Rawat,
|
|
11
Rajin),
DCC
(Dankos
Customer
Care)
di seluruh
bagian.
Selain
itu
Dankos
menjadi
Industri
farmasi Indonesia
yang
mampu
memproduksi
obat
soft
capsule.
Pada
bulan
Juli
2004
Dankos
memperoleh
sertifikat
ISO
14001
mengenai
mutu
lingkungan
dan
pengolahan
limbah
cair.
Kemudian pada
bulan
September
2004
Dankos
memperoleh
sertifikat
OHSAS
(sertifikat
mengenai
K3),
untuk
menjaga
serta
meningkatkan
keselam atan
dan
kesehatan
lingkungan
kerja.
1.5.2
Profil Perseroan
PT.Dankos Laboratories Tbk
m
erupakan perusahaan
farmasi
PMDN
terkemuka
di
Indonesia,
dan
sebagai perusahaan
Go
Publik sejak
tahun
1989,
dimana
secara
konsisten
menerapkan
CPOB
dan
ISO
9001 dalam
memproduksi
obat-
obatan
(obat
resep
dan
obat bebas),
serta
memiliki
pemasaran
di
dalam
dan
luar
negeri.
Perseroan
di
tahun
2000
ini
telah
menguasai
6,59
%
pasar
farmasi
Indonesia
yang
terdiri
dari
13,36
%
pasar
obat
bebas
dan
2,12
%
pasar
obat
resep,
melalui
perusahaan
ini
sendiri
dan
tiga anak perusahaan,
yaitu
:
1.
PT. Bintang
Toedjoe,
dimana produk
yang dihasilkan antara
lain Extra
Joss, Kom ix, Waisan.
2.
PT.
Hexpharm
Jaya
Laboratorios,
dim ana produk
yang dihasilkan
antara lain
ATP Kyowa, Spasminal, dan Benacol.
|
|
12
3.
PT.
Saka
Farma
Laboratories,
dimana
produk
yang
dihasilkan
antara
lain
Sakatonik
ABC, Sakatonik
Liver
dan Mextril.
Pada tahun
2005 PT.
Dankos
Laboratories Tbk
melakukan
merger dengan
2
perusahaan
besar
yaitu PT.
Kalbe
Farma
Tbk
dan
PT. Enseval
Tbk. PT.
Dankos
Laboratories
Tbk
berganti
nama
menjadi
PT.
Buana
Inti
Cermelang.
Pada
tanggal
1
January
2007,
Perusahaan
ini
berganti
nama
lagi
menjadi
PT.
Dankos
Farma
yang
merupakan
Bisnis
Operasional
dari
PT. Kalbe
Farma
Tbk.
Dengan
merger
ini
perusahaan
Kalbe
Farma
yang
m
enjadi
induk
pasca
merger
merupakan
perusahaan
farmasai
terbesar
di
Indonesia
bahkan
di
Asia
Tenggara.
1.5.3
Kebijakan M utu
Kebijakan
Mutu
Perusahaan
ini
adalah
" Kami,
manajemen
dan segenap
karyawan PT.
Dankos
Laboratories
mempunyai
kom itm en
untuk
menghasilkan
produk
kesehatan
yang
bermutu
melalui:
Dedikasi
yang
tinggi
untuk
mencapai
mutu
dengan
Aktif
dan
terus
menerus
memahami
kebutuhan
konsumen
serta
Niat
yang
kuat
untuk
menghasilkan
produk
dengan
Kualitas
yang
Optimal
melalui
penerapan
Sistem
CPOB
(Cara
Pembuatan
Obat
yang
Baik), ISO 9001 dan Perbaikan
yang berkesinambungan".
Untuk
melengkapi
CPOB
dan
ISO
9001
yang
telah
diperoleh,
pada
bulan
Januari
2000
juga
telah
memperoleh
sertifikat SMK3
(Sistem
Manajemen
Keselamatan
Kesehatan
Kerja)
dari
PT.
Sucofindo.
Perseroan
dan
anak
|
 13
perusahaan
Perseroan
secara
konsisten
menerapkan
CPOB
(Cara
Pembuatan
Obat
yang
Baik)
dan
ISO
9001.
Di
samping
itu
sejak
tahun
2000
juga
telah
secara
terus
m
enerus
menerapkan
sejum ah
lah
"Best
Practice"
yaitu
perbaikan
yang berkesinambungan,
kepuasan
pelanggan,
5R
(Ringkas,
Rapi,
Resik,
Rawat dan
Rajin)
dan
pelatihan, sehingga akhirnya
dapat
m
enjadi
budaya
Perseroan.
Hal
ini sesuai
dengan
visi
Perseroan
yang senantiasa
menjadi
perusahaan
farmasi yang
m
empunyai komitmen
kuat
untuk
meningkatkan
kesejahteraan masyarakat
m
elalui
penerapan
ilmu dan teknologi
di tingkat
nasional dan regional
serta sebagai pemberi
kerja terbaik
di Indonesia.
Disamping
itu
juga
sejalan
dengan
m si
isi
Perseroan
yaitu
sebagai
sebuah
grup
perusahaan
yang
senantiasa
melakukan perbaikan yang berkesinambungan
untuk
menghasilkan
produk
kesehatan
yang
berkualitas
melalui
pengembangan
produk yang
inovatif,
mudah
diperoleh
dan
terjangkau
oleh
masyarakat
luas
sehingga
ikut
berperan
serta
dalam
meningkatkan
kesejahteraan
masyarakat.
Gb 1.1 Gambar
Dankos
Quality Excellence dengan
Best
Practice-nya
|
|
14
1.5.4
Pengaturan Jam
Kerja
PT.
Dankos
Farma
mempunyai
peraturan
untuk
jam
kerja dengan
menyesuaikan
kebutuhan
produksi
itu
sendiri.
Untuk
normalnya kegiatan
produksi
dilakukan
secara
2 shift
dan
apabila
permintaan
produksi
sangat
banyak, kegiatan produksi bisa dilakukan secara
long shift.
Hari
kerja
di
PT. Dankos
Farm a
adalah
Senin
–
Jumat
dengan pembagian
waktu kerja sebagai
berikut
:
•
Karyawan
Kantor
Jam kerja
:
07.00 –
15.30
WIB
•
Karyawan
Lantai
Produksi
dan
Gudang
Shift I
: 07.00 –
15.30
WIB
Shift II
: 15.30 –
22.50
WIB
Long
Shift I
: 07.00 –
19.30 WIB
Long Shift II : 19.30 –
07.00
WIB
Untuk
jam
kerja
normal
kegiatan
produksi
diatas
dilakukan dengan
istirahat
selama
30
m
enit
disetiap
shiftnya.
Dan
untuk longshift
dilakukan
selama
2
kali.
Beberapa
kali
juga
diperlukan kegiatan
produksi
dilakukan
pada
waktu
hari
Sabtu
dan
Minggu
secara overt ime
sesuai
dengan
permintaan
produksi itu
sendiri.
|
|
15
1.5.5 Produk-produk
yang dihasilkan
Produk
yang
dihasilkan
oleh
PT.
Dankos
farm a
dibagi
berdasarkan
kategori
pemasaran.
Yaitu
produk
obat
bebas
(Over
The
Counter)
:
Mixagrip,
Fatigon,
Fatigon
Spirit,
Fatigon
Viro,
Mixadin,
Minigrip,
Extra
Joss,
Kom
ix,
OSK,
Irex,
Joss
Kid,
Sakatonik,
Mextril,
Sakatonik
ABC,
Sakatonik
Grenk,
Sakatonik
Kaplet
dll.
Berikutnya
obat-obat
resep
(Ethical)
:
Neurotam,
Cefizox,
Brainact,
Reskuin,
Cefazol, Fixef, Mikasin,
Spiradan,
Foxim, Digest, Cefotaxime,
Bintamox,
Ceftriaxone,
Sakaneuron,
Dextromethorphan
dll.
1.5.6 Jaringan Penjualan
PT.
Dankos
Farma
mempunyai jaringan
penjualan
untuk
dalam
negeri
(domestic)
dan
juga
penjualan
yang
dikhususkan
untuk
ekspor
kebeberapa
negara
seperti
Malaysia,
Myanmar,
Filipina,
Singapura,
Kamboja,
Thailand,
Sri
Lanka,
Mongolia,
Hongkong,
Afrika Selatan, Nigeria & Zimbabwe.
1.5.7 Fasilitas Perusahaan
•
Sebagai
salah
satu
perusahaan
farmasi
besar
di
Indonesia
yang
kemudian
bergabung menjadi Kalbe
Farma menjadi
terbesar
se-Asia Tenggara.
•
Investasi
dalam
fasilitas
manufaktur
dan
pendukung
yang
terus
dikembangkan.
•
Mempunyai
dukungan
fasilitas
penunjang
yang
lengkap
:
penelitian
dan
pengembangan,
pelatihan
khusus dan
fasilitas pengujian
modern
|
|
16
•
Mempunyai
gedung
terpisah
untuk
produksi
Obat
kategori Penicillin,
Cephalosporin
dan
Non
Beta
Laktam.
Fungsi
gedung
terpisah
ini
sesuai
dengan
peraturan
dari
GMP (Good
Manufaturing
Product)
Farmasi
untuk
menghindari kontaminasi
antara
jenis karakteristik obat
yang berbeda.
Untuk
mendalaim i pabrik
untuk
obat- obatan
golongan
Beta Laktam dapat
dilihat
diuraian berikut :
a.
Pabrik
untuk Obat- obatan
golongan
Beta Laktam Penicillin
Pabrik
ini
dibangun
hanya khusus
untuk
membuat
obat-
obatan
golongan
Penicillin.
Obat-
obat
golongan
Penicillin
ini
harus
dibuat
terpisah
sama
sekali
dari
obat-
obat
lain
karena
kalau
tidak
obat-
obat
lain
dapat
terkontaminasi oleh
Penicillin.
Obat-
obat
golongan
ini
sangat
berbahaya
bagi
orang-
orang
yang alergi
terhadap
obat
ini.
Bentuk
sediaan
yang dibuat di pabrik
ini, yaitu :
o
Tablet Inti (Plain
Tablet)
o
Tablet Salut Selaput (Film
Coated Tablet)
o
Sirup
Kering (Dry Syrup)
b. Pabrik
untuk
Obat- obatan
golongan
Beta Laktam Cephalosporin
Pabrik
ini
dibangun
khusus
untuk
m
embuat
obat-
obat
golongan
Beta Laktam Cephalosporin. Obat ini
juga
dapat
m
enimbulkan
alergi, meski
efeknya tidak sedahsyat
Penicilin
karena
obat
|
|
17
golongan
ini terkadang
diberikan
untuk
pasien
yang
tidak
tahan
terhadap
penicillin.
Bentuk
sediaan
yang dibuat di pabrik
ini, yaitu :
o
Tablet Inti (Plain
Tablet)
o
Tablet Salut Selaput (Film
Coated Tablet)
o
Sirup
Kering (Dry Syrup)
o
Kapsul
Keras (Hard
Capsule)
o
Injeksi
Serbuk (Powder Injection)
|
 18
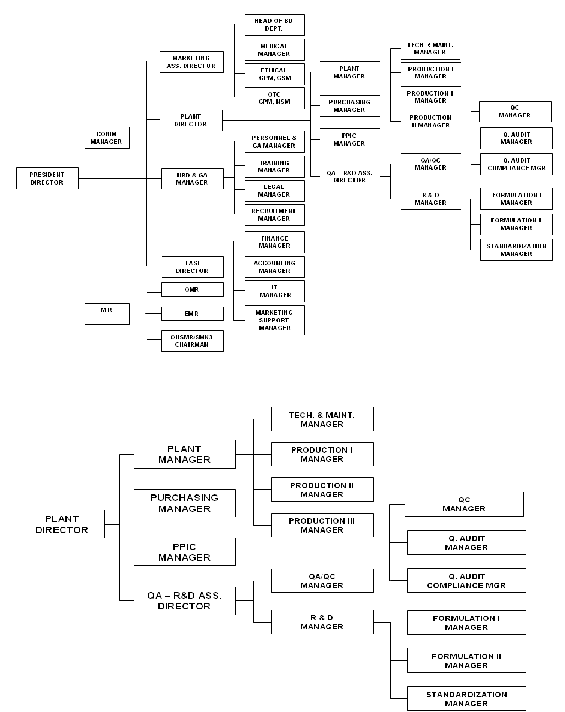
1.5.8
Struktur
Organisasi
1.5.8.1 Struktur Organisasi PT. Dankos
Farma
1.5.8.2 Struktur Organisasi Plant
PT. Dankos Farma
|
|
19
1.5.9
Proses Produksi
1.5.9.1 Proses Produksi Tablet/ Kaplet Inti
Langkah-
langkah
cara pembuatan
tablet/ kaplet inti adalah
:
•
Penimbangan
Bahan obat dari gudang bahan baku ditimbang sesuai formula
dan
prosedur
(bila perlu
diayak dahulu).
•
Granulasi
Pada proses
granulasi basah
dilakukan
pembuatan bahan
pengikat
serbuk,
kemudian dicampur
dengan bahan
obat sehingga terbentuk
massa granul
basah.
Kemudian
diayak dan
keringkan
sehingga
mencapai kadar
air tertentu dalam fluid
belt dryer,
lalu diayak
lagi.
Pada proses
granulasi kering bahan-
bahan
obat di slugging,
lalu
diayak.
•
Lubrikasi
Granul kering yang terbentuk pada proses granulasi basah atau
gaanulasi kering,
atau bahan
obat untuk
cetak
langsung dimasukan
ke dalam
mixer
dan
dicampur
dengan pelicin (lubricant).
•
Pencetakan
Hasil
lubrikasi dicetak dalam mesin
cetak.
•
Penyetripan
(Stripping)
|
 20
Tablet/ kapsul dimasukkan
ke dalam hopper mesin
stripping
untuk
dilakukan penyetripan.
•
Pengemasan
Strip-
strip diberi catch
cover dengan mesin dan di kemas
dalam
individual box,
lalu diberi kartu kontrol
dan dimasukkan ke dalam
master box yang disegel.
Hasil pengemasan dikirim ke gudang obat
jadi.
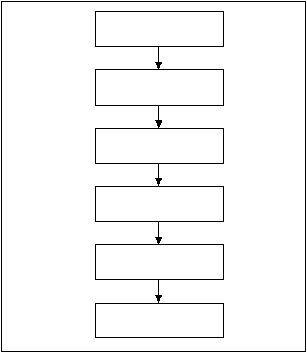
Penimbangan
Granulasi
Lubrikasi
Pencetakan
Penyetripan
Pengemasan
Gb 1.2 Tahapan
Proses Produksi Kaplet Inti
1.5.9.2 Proses Produksi Tablet
Salut
Langkah-
langkah
pembuatan Tablet
Salut adalah
:
•
Penyalutan
|
 21
Buat
larutan
penyalut sesuai
dengan formula.
Tablet
yang akan
disalut dimasukkan
ke dalam mesin film coating/
coating
pan,
kemudian dilakukan
penyalutan sesuai prosedur.
•
Polishing
Tablet yang
akan disalut
gula dimasukkan ke dalam polishing drum
untuk
selanjutnya dilapis dengan
larutan polishing.
•
Penyetripan/
Stripping
Sama
seperti pada penyetripan
tablet/
kaplet biasa.
•
Pengemasan
Sama
seperti pengemasan tablet/ kaplet.
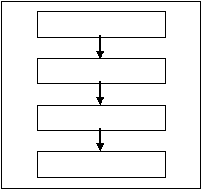
Penyalutan
Po ishing
lishing
Penyetrip an
Pengemas an
Gb 1.3 Tahapan
Proses Produksi Kaplet Salut
1.5.9.3 Proses Produksi Kapsul Keras
Langkah-
langkah cara pembuatan kapsul
keras
:
•
Penimbangan
Bahan-
bahan
obat
ditimbang sesuai formula prosedur
yang
ditetapkan.
|
 22
•
Pencampuran
Bahan-
bahan obat
dimasukkan
ke dalam
mixer
kemudian
dicampur
sampai
homogen.
•
Pengisian dan Penutupan
Masukkan
kapsul
kosong ke dalam
mesin
pengisi
kapsul.
Bahan
obat
yang sudah
dicampur
dimasukkan
ke dalam
hopper
mesin,
kemudian
dilakukan pengisian
dan
penutupan
kapsul.
•
Penyetripan
Kapsul-
ckapsul
yang
telag
terisi
dimasukkan
ke
dalam
hopper
mesin strip un tuk
dilakukan
penyetripan.
•
Pengemasan
Strip-
strip
dikemas
dalam
individual
box,
lalu
diberi
kartu
kontrol
dan
dimasukkan
ke
dalam
master
box
yang disegel.
Hasil
pengemasan dikirim
ke
gudang obat
jadi.
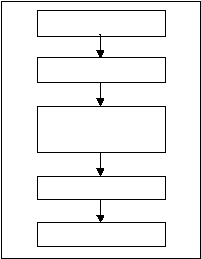
Penimbangan
Penc amp uran
Pengisian &
Penutupan
Penyetrip an
Pengemas an
|
|
23
Gb 1.4
Tahapan Proses
Produksi
Kapsul Keras
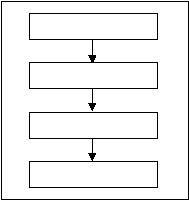
1.5.9.4 Proses Produksi Sirup
Kering
Langkah-
langkah cara pembuatan sirup
kering
:
•
Penimbangan
Bahan- bahan
obat ditimbang sesuai formula prosedur
yang
ditetapkan.
•
Pencampuran
Bahan-
bahan obat dimasukkan
ke
dalam
mixer kemudian
dicampur
sampai
homogen.
•
Pengisian
Bahan obat dimasukkan ke dalam hopperb
mesin
pengisi,
lalu
diisi
ke dalam
botol.
•
Pengmasan
Botol
yang telah
berisi sirup
kering di pasang etiket dan dimasukkan
ke dalam
doos kecil
dan dilengkapi
dengan brosur.
Kemudian
dimasukkan
ke
dalam
individual
box.
Hasil pengemasan di kirim
ke
gudang obat jadi.
|
 24
Penyalutan
Polis hing
Penyetrip an
Pengemas an
Gb 1.5 Tahapan
Proses Produksi Sirup
Kering
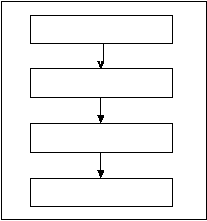
1.5.9.5
Proses Produksi Injeksi Kering
Langkah-
langkah
proses pembuatan injeksi
kering:
•
Sterilisasi
Sebelum
proses produksi dimulai terlebih dahulu
dilakukan
sterilisasi ruangan,
mesin,
wadah
dan
perlengkapannya.
•
Pengisian
Vial
yang telah
bersih dan
steril
diisi serbuk
steril dengan
menggunakan mesin pengisi lalu
ditutup.
•
Pemeriksaan
Visual
Vial yang telah
bwerisi
serbuk diperiksa secara visual untuk melihat
ada tidaknya partikel atau serat.
•
Pengemasan
|
 25
Vial-
vial dimasukkan ke dalam doos kecil dan dilengkapi dengan
brosur.
Kemudian dimasukkan ke dalam individula box, duberi kartu
kontrol dan dimasukkan
ke dalam master
box,
segel.
Sterilisas
i
Pengisian
Pemeriks aan Visual
Pengemas an
Gb 1.6 Tahapan Proses Produksi Injeksi
Kering
|